作為國內(nèi)最早成功輔導(dǎo)企業(yè)采用醫(yī)療器械注冊(cè)人制度?完成產(chǎn)品注冊(cè)的第三方醫(yī)療器械咨詢公司之一���,作為輔導(dǎo)浙江省首2家采用醫(yī)療器械注冊(cè)人制度并順利通過體考的第三方醫(yī)療器械咨詢公司���,杭州證標(biāo)客醫(yī)藥技術(shù)咨詢有限公司帶大家一起來了解MAH制度下,體系考核注意事項(xiàng)����。
作為國內(nèi)最早成功輔導(dǎo)企業(yè)采用醫(yī)療器械注冊(cè)人制度完成產(chǎn)品注冊(cè)的第三方醫(yī)療器械咨詢公司之一,作為輔導(dǎo)浙江省首2家采用醫(yī)療器械注冊(cè)人制度并順利通過體考的第三方醫(yī)療器械咨詢公司�,杭州證標(biāo)客醫(yī)藥技術(shù)咨詢有限公司帶大家一起來了解MAH制度下��,體系考核注意事項(xiàng)�����。
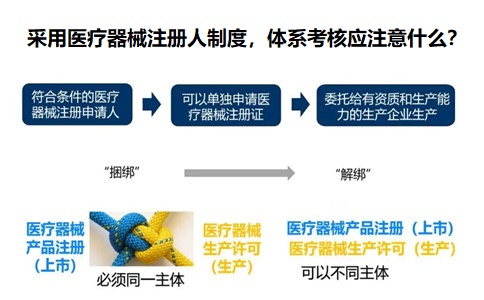
采用醫(yī)療器械注冊(cè)人制度�,體系考核應(yīng)注意什么�?
委托生產(chǎn)前,醫(yī)療器械注冊(cè)申請(qǐng)人應(yīng)當(dāng)對(duì)受托生產(chǎn)企業(yè)的質(zhì)量管理體系開展現(xiàn)場(chǎng)評(píng)估審核��,審核內(nèi)容至少應(yīng)當(dāng)包括機(jī)構(gòu)和人員�、廠房與設(shè)施、設(shè)備��、生產(chǎn)管理���、質(zhì)量控制能力等�����,確保受托生產(chǎn)企業(yè)具備與受托生產(chǎn)產(chǎn)品相適應(yīng)的質(zhì)量管理體系����。
申請(qǐng)人應(yīng)當(dāng)定期對(duì)受托生產(chǎn)企業(yè)的受托生產(chǎn)管理情況和相關(guān)記錄進(jìn)行審核���,并保留審核記錄�。受托生產(chǎn)企業(yè)應(yīng)當(dāng)保留受托生產(chǎn)相關(guān)的全部生產(chǎn)記錄,并可隨時(shí)提供給申請(qǐng)人備查�。如果受托生產(chǎn)企業(yè)有相同產(chǎn)品在生產(chǎn),應(yīng)當(dāng)與受托生產(chǎn)產(chǎn)品有顯著區(qū)別的編號(hào)����、批號(hào)及過程標(biāo)識(shí)管理方式,避免混淆����。